打开文本图片集
[摘要]目的 探讨乳腺癌新辅助治疗病理完全缓解的影响因素及预后。方法 回顾性分析2010年6月12日~2015年6月12日新疆维吾尔自治区人民医院收治的150例乳腺癌患者的临床资料,所有患者均为女性,均接受新辅助化疗,对其临床资料、病理资料、随访资料进行收集分析,探讨病理完全缓解的影响因素及预后。结果 患者体质量、哺乳时间、化疗周期、肿瘤大小、雌激素受体(ER)、孕激素受体(PR)、雌/孕激素受体(ER/PR)、分子分型均为影响新辅助治疗病理完全缓解的单因素,经Logistic回归分析可知,体质量、ER均为影响新辅助治疗病理完全缓解的独立预测因素,新辅助治疗病理完全缓解对乳腺癌患者生存无明显影响。结论 对于乳腺癌患者,其体质量、ER均为乳腺癌新辅助治疗病理完全缓解的影响独立预测因素,而且新辅助治疗病理完全缓解与乳腺癌患者的预后生存无明显影响。
[关键词]影响因素;预后;新辅助治疗;乳腺癌;病理;完全缓解
[中图分类号] R737.9 [文獻标识码] A [文章编号] 1674-4721(2019)2(b)-0095-03
乳腺癌为临床常见恶性肿瘤疾病类型,在女性人群中,其发生率占第一位。新辅助治疗与新辅助治疗预后关系是目前临床乳腺外科重要的关注问题[1]。病理完全缓解是属于临床乳腺癌患者新辅助化疗预后的重要评价指标[2]。对于局部进展期的乳腺癌患者而言,新辅助治疗属于标准的治疗方案;对于早期病变患者而言,可给予手术进行治疗,以提高治疗的成功率。新辅助治疗与原发病灶病理完全缓解率、生存情况等的联系紧密,将会影响到患者的预后[3-4]。本研究旨在探讨乳腺癌新辅助治疗病理完全缓解的影响因素及预后,现报道如下。
1资料与方法
1.1一般资料
回顾性分析2010年6月12日~2015年6月12日新疆维吾尔自治区人民医院收治的150例乳腺癌患者的临床资料,均接受新辅助化疗。所有患者对本次研究均知情同意,均获得了明确的诊断,具有完整的病理资料。所有患者均为女性,年龄为23~69岁,平均(45.23±3.15)岁,手术治疗前给予B超检查,排除伴有远处转移的患者。本研究经医院医学伦理委员会审核批准。
1.2方法
对所有患者均采取新辅助化疗的方式,治疗周期为4~8个,包括蒽环类方案、紫衫类方案、蒽环类与紫衫类序贯治疗、蒽环或紫杉醇序贯其他治疗方案,之后采取手术进行治疗。150例患者中,62例采取乳腺癌局部扩大切除术+腋窝淋巴结清扫术,88例采取改良根治术进行治疗,之后102例患者由于术前化疗时间低于8个周期,采取辅助化疗模式,原发灶病理完全缓解患者给予新辅助化疗,原发灶残留患者给予新辅助化疗不同方案进行干预,若新辅助化疗周期为8个,手术后无需给予辅助化疗。
1.3观察指标与判定标准
收集150例乳腺癌患者的一般资料(包括年龄、体质量、身高、哺乳情况、月经情况、既往史、家族史等)、B超等辅助检查结果以及手术资料(包括治疗方式、肿瘤大小、病理类型、淋巴结转移等)。分析腋窝阳性淋巴结病理完全缓解的判定标准为:术后病理检查腋窝淋巴结情况未累及癌;1年无远处转移生存(1年DDFS)是指新辅助化疗1年内未出现远处转移病灶或者乳腺癌相关性死亡情况[5-7]。
1.4统计学方法
采用SPSS 21.0统计学软件对数据进行分析,计量资料以均数±标准差(x±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,临床病理特征以及病理完全缓解的相关性多因素分析均使用Logistic回归分析方法,生存相关多因素分析使用COX风险回归模型,影响生存危险因素分析使用后退法筛选方法,存活率使用Kaplan-Meier曲线进行计算,生存差异比较使用差异Log-rank检验方法,通过双侧检验,以P<0.05为差异有统计学意义。
2结果
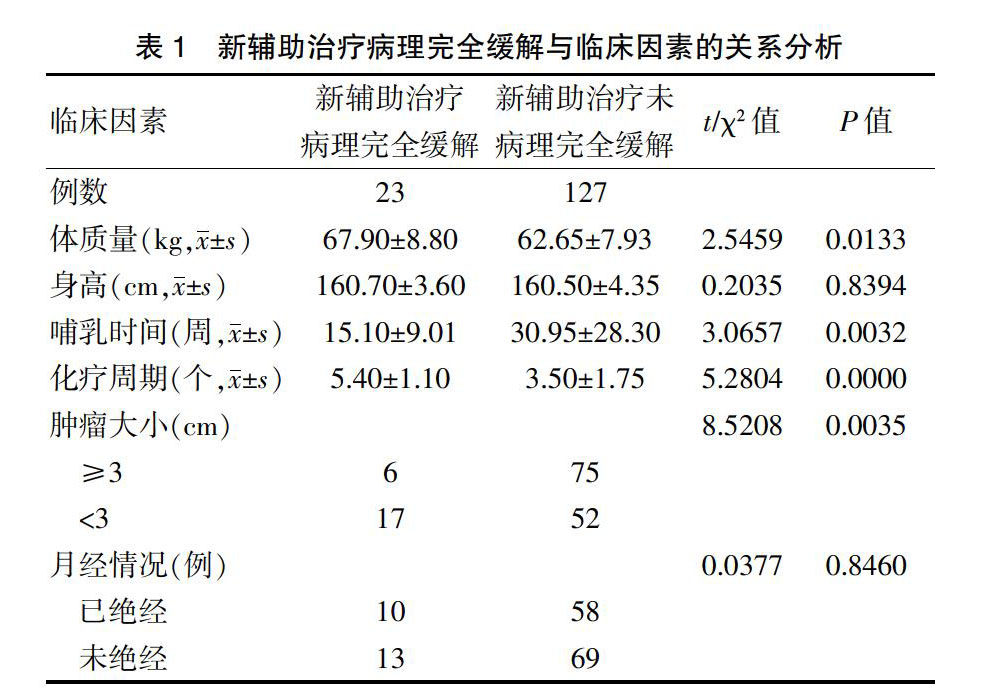
2.1新辅助治疗病理完全缓解与临床因素的关系分析
新辅助治疗病理完全缓解与患者体质量、哺乳时间、化疗周期、肿瘤大小等临床因素有关,新辅助治疗病理完全缓解与患者身高、月经情况等临床因素无关(表1)。
2.2新辅助治疗病理完全缓解与病理指标的关系分析
经分析,新辅助治疗病理完全缓解与患者雌激素受体(ER)、孕激素受体(PR)、雌/孕激素受体(ER/PR)、分子分型等病理指标有关,新辅助治疗病理完全缓解与患者Ki-67比例、组织学分级等病理指标无关(表2)。
2.3新辅助治疗病理完全缓解Logistic回归分析
Logistic回归分析显示,患者的体质量及患者ER是新辅助治疗病理完全缓解的独立预测因素(表3)。
2.4新辅助治疗病理完全缓解对乳腺癌患者生存的影响分析
参与本次研究的150例乳腺癌患者经持续跟踪随访1~3年,平均跟踪随访时间为(30.50±1.50)个月;随访结果可知,死亡12例,远处转移(或局部复发)28例。23例新辅助治疗病理完全缓解患者中,死亡0例,远处转移(或局部复发)3例;127例新辅助治疗未病理完全缓解患者中,死亡12例,远处转移(或局部复发)25例。新辅助治疗病理完全缓解患者与新辅助治疗未病理完全缓解患者的总生存期及无病生存期比较,差异无统计学意义(P>0.05)。
3讨论
乳腺癌属于恶性肿瘤疾病类型,其发生率占女性恶性肿瘤第一位。新辅助治疗乳腺癌与治疗预后关系已成为目前临床乳腺外科的热点关注问题[8-9]。有关学者研究显示[10-11],对乳腺癌患者给予新辅助化疗模式后,其原发灶病理缓解情况和预后的联系较为紧密,所以说,病理的缓解率可作为该类疾病患者新辅助化疗效果判定的重要因素。
病理完全缓解即原发病灶未见肿瘤病灶、淋巴结未见肿瘤病灶,或者原发病灶与淋巴结均仅有原位癌残留[12]。病理完全缓解主要用于乳腺癌新辅助治疗预后的评价指标之一,且占据着重要作用价值。相关研究发现,乳腺癌患者接受新辅助治疗后,若达到病理完全缓解,则可以获得更长生存获益。但是新辅助治疗后达到病理完全缓解的乳腺癌患者仅占少部分,而有部分乳腺癌患者在接受新辅助治疗时,病情持续发展,导致丧失早期手术机会;其次,还有部分乳腺癌患者出现耐药反应[13-14]。本研究结果显示,乳腺癌新辅助治疗病理完全缓解患者的临床因素(包括体质量、哺乳时间、化疗周期、肿瘤大小)以及病理指标(包括ER、PR、ER/PR、分子分型)均有明显差异性(P<0.05);除此之外,乳腺癌新辅助治疗病理完全缓解患者的体质量及ER均可作为独立预测因素;其次,乳腺癌患者新輔助治疗病理完全缓解的总生存期及无病生存期与乳腺癌新辅助治疗未病理完全缓解患者无明显差异性(P>0.05),提示新辅助化疗病理完全缓解的独立预测因素主要包括乳腺癌患者的体质量以及ER,其次新辅助化疗病理完全缓解与乳腺癌患者的生存无明显影响性[15-16]。
综上所述,乳腺癌新辅助治疗病理完全缓解影响因素主要包括乳腺癌患者体质量、ER,而病理完全缓解与患者预后生存无明显影响。
[参考文献]
[1]何英剑,李晓婷,范照青,等.应用决策曲线方法评价乳腺癌新辅助治疗后病理完全缓解的MRI早期预测模型[J].中华医学杂志,2018,98(4):260-263.
[2]刘伟,李健斌,王涛,等.乳腺癌分子亚型与新辅助化疗疗效及预后的相关性分析[J].中华医学杂志,2016,96(36):2898-2902.
[3]李志红,刘丹,何自静,等.地塞米松对新辅助化疗后乳腺癌患者术后恶心呕吐发生率的影响[J].北京大学学报(医学版),2015,47(4):685-689.
[4]韩忠华,林舜国,许春森,等.三阴性乳腺癌新辅助化疗后淋巴结阴性原发灶癌残留的影响因素分析[J].中国现代医生,2017,55(34):81-83,87.
[5]程元甲,叶京明,徐玲,等.乳腺癌新辅助治疗病理完全缓解预测因素分析[J].中华外科杂志,2013,51(4):339-343.
[6]石爱平,徐格格,解新鹏,等.St.Gallen会议乳腺癌新辅助治疗回顾[J].山东大学学报(医学版),2018,56(1):6-11,21.
[7]刘世伟,徐玲,张虹,等.HER2阳性乳腺癌新辅助治疗病理完全缓解预测因素分析[J].中华外科杂志,2016,54(2):94-98.
[8]庞丹梅,温灵珠.卡铂新辅助治疗可提高早期三阴性乳腺癌患者的病理完全缓解率[J].循证医学,2017,17(3):150-152.
[9]宋金洁,王涛,边莉,等.曲妥珠单抗联合蒽环类药物应用于Her-2阳性乳腺癌的新辅助治疗初步临床研究[J].实用肿瘤学杂志,2013,27(2):97-100.
[10]姚和瑞,游凯云,汪颖,等.CALGB 40603研究分析:Ⅱ/Ⅲ期三阴性乳腺癌新辅助化疗加用卡铂和/或贝伐单抗提高病理完全缓解率[J].循证医学,2017,17(3):140-145.
[11]张香梅,曹淼,刘北辰,等.恩度联合TEC方案新辅助治疗Ⅲ期乳腺癌临床研究[J].中华肿瘤防治杂志,2018,25(4):258-262.
[12]韩瑞,王冠英,张玉姣,等.贝伐珠单克隆抗体联合化疗用于Her2阴性乳腺癌患者新辅助治疗的meta分析[J].浙江大学学报(医学版),2016,45(4):379-386.
[13]宋云骏,姜林鹤,刘运江,等.CD133在乳腺癌新辅助化疗后的表达及其临床意义[J].临床和实验医学杂志,2014, 13(4):297-300.
[14]张钢龄,张培礼,朱敬军,等.紫杉醇联合卡铂单周新辅助化疗加曲妥珠单抗在HER2阳性乳腺癌的探讨[J].中国中西医结合外科杂志,2015,21(5):463-466.
[15]刘文清,叶京明,徐玲,等.分子分型及动态增强磁共振成像对乳腺癌新辅助治疗疗效的预测和评价[J].中华外科杂志,2013,51(8):706-709.
[16]赵迎春,李勇,朱永云,等.乳腺癌分子亚型在预测新辅助化疗疗效及患者预后中的作用[J].国际外科学杂志,2016,43(3):162-166,封3.
(收稿日期:2018-09-04 本文编辑:祁海文)







